Lo invitamos a leer los Lineamientos para el uso de pruebas diagnósticas de laboratorio durante la pandemia del SARS-CoV-2 (COVID-19) en Colombia dados por el Ministerio de Salud.
A continuación le damos un resumen sobre las pruebas rápidas que el laboratorio está manejando.
- Definición de pruebas rápidas basadas en detección de anticuerpos:
Se trata de pruebas rápidas que detectan la presencia de anticuerpos IgM/IgG como respuesta inmunológica durante las diferentes fases de la infección.
Las pruebas rápidas serológicas de anticuerpos IgM/IgG se indican para identificar el contacto previo de una persona con el virus SARS-CoV2.
- Pruebas rápidas serológicas (anticuerpos IgM/ IgG)
Las pruebas rápidas serológicas de anticuerpos IgM/IgG se indican para identificar el contacto previo de una persona con el virus SARS-CoV2. No se consideran pruebas diagnósticas y no se recomienda su uso para descartar un caso de infección aguda.
- Persona con síntomas leves mayor a 10 días y sin factores de riesgo.
- Contacto estrecho con síntomas leves mayor a 10 días y sin factor de riesgo.
- Persona asintomática con o sin factores de riesgo.
- Personas con criterio 1 Y 2
- Realizar prueba rápida de anticuerpos IgM/ IgG que cumpla los criterios del Ministerio, después de 10 días del inicio de los síntomas.
- Si la prueba rápida de anticuerpos IgM/IgG es positiva, se requiere aislamiento obligatorio y estricto por 14 días, estudio de contacto y seguimiento cercano de su evolución clínica.
- Si esta prueba rápida de anticuerpos IgM/IgG es negativa, se debe ordenar aislamiento de la persona por 14 días.
- Persona asintomática con o sin factores de riesgo
- Realizar prueba rápida de anticuerpos IgM/IgG a los 14 días de la cuarentena. Si el resultado de la prueba es positivo continuar en la comunidad, si es negativa continuar en la comunidad con medidas de prevención y de acuerdo con riesgo individual ordenar nueva prueba rápida de anticuerpos IgM/IgG de 2 a 4 semanas.
- Uso de pruebas rápidas de detección de Anticuerpos en Emergencia en Salud Pública
- Cualquier prueba rápida que vaya a ser usada deberá cumplir con los criterios emitidos por el Ministerio de Salud y Protección Social.
- A continuación, se presenta infografía con la interpretación del significado clínico de acuerdo con el resultado de pruebas rápidas serológicas de anticuerpos IgM/IgM y RT-PCR SARS CoV 2.
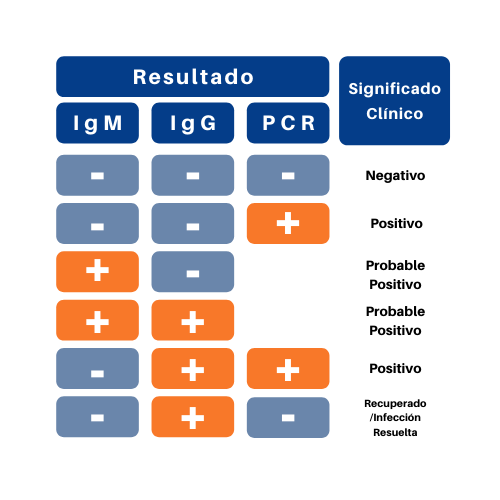
- Tamizajes poblacionales
Referente al tamizaje de conglomerados poblacionales es necesario tener en cuenta que tienen el objetivo de observar cómo se está comportando la transmisión del virus en grupos poblacionales específicos.
En consecuencia, no se enmarcan en las atenciones individuales, sino por el contrario, corresponden a estrategias de salud pública colectivas.
- Las pruebas RT-PCR podrán ser adquiridas y únicamente realizadas por entidades que cuenten con un laboratorio autorizado por el INS o que hayan llegado a acuerdos con alguno de estos laboratorios para la realización de este tipo de pruebas.
- Las pruebas rápidas serológicas (anticuerpos IgG/IgM) podrán ser utilizadas para realizar estudios de vigilancia epidemiológica o para inferir seroprevalencia en un sitio o área determinada.
- Las empresas públicas o privadas podrán financiar estas pruebas para sus trabajadores, siguiendo los lineamientos que se definen para cada grupo poblacional y garantizando que estén autorizadas por la autoridad competente y previamente validadas.
Seroprevalencia: Manifestación general de una enfermedad o una afección dentro de una población definida en un momento dado, medida con análisis de sangre (pruebas serológicas).
- Consideraciones en la adquisición de pruebas
En caso de ser pruebas de anticuerpos IgG/IgM se deberá tener en cuenta que, como mínimo, debe cumplir con lo siguiente:
- Reportar sensibilidad y especificidad por encima del 80%.
- Un reporte sobre el porcentaje de correlación (tasa de coincidencia) con la PCR, mayor del 80%.
- Que tenga en cuenta el número de muestras con el cual la casa comercial hizo la validación (mínimo 100).
Categorías
- Científicas (27)
- Seguridad y salud en el trabajo (3)
- Novedades (3)






Participe y comente esta publicación: